北京维通达生物科技有限公司宣布已与北京协和医院完成科研成果转化签约,正式取得由北京协和医院团队研发的胰腺导管内乳头状黏液性肿瘤(IPMN)模型小鼠及其制备技术的授权与技术转让。此项合作标志着维通达在肿瘤动物模型领域再添重磅技术,进一步夯实从临床科研到产业转化的全链条服务能力。
治疗胰腺癌药物成果新进展
2026年4月17日-22日第117届美国癌症研究协会(AACR)年会在美国加利福尼亚州圣地亚哥举行,贝达药业泛KRAS降解剂BPI-585771的临床前研究数据在本次会议亮相,结果显示BPI-585771对KRASG12D驱动的胰腺癌模型具有显著治疗效果。同月,由美国纪念斯隆凯特琳癌症中心Wungki Park多位研究者在《New England Journal of Medicine》上发表了题为“Setidegrasib in Advanced Non-Small-Cell Lung Cancer and Pancreatic Cancer ”的研究论文。该研究首次公布了KRAS G12D选择性蛋白降解剂Setidegrasib(ASP3082)在晚期实体瘤患者(胰腺癌)中的I期临床数据,验证了通过PROTAC技术“降解”而非“抑制”突变KRAS蛋白的治疗策略的可行性、安全性和初步抗肿瘤活性。
多样化临床自发胰腺癌类型需求
尽管 KRAS 靶向降解等创新疗法已在临床前与早期临床中展现出巨大潜力,但胰腺导管腺癌(PDAC)极高的恶性程度与复杂的细胞起源异质性,仍极大制约了新药研发与临床转化效率。而可靠的、能精准模拟不同细胞起源与疾病进程的胰腺癌动物模型,正是连接基础机制研究与临床治疗突破的关键桥梁。虽然目前认为腺泡细胞和导管细胞都是胰腺癌的可能起源,但它们各自对应的PDAC亚型临床及分子特征仍不清楚。腺泡细胞衍生的PDAC,通常认为经历腺泡导管化生(ADM),目前已有大量研究使用 Pdx1-Cre 或 Ptf1a-Cre 等模型进行了充分研究。导管细胞也是胰腺癌的潜在发生细胞,以胰腺导管内乳头状黏液性肿瘤(IPMN)为代表。这是一类通过影像学检查可以早期发现和识别的胰腺癌癌前病变,被认为是PDAC早期诊断的重要窗口。然而,针对IPMN及导管细胞来源PDAC的模型的报道与研究仍十分匮乏。
最新发表文章解读
中国医学科学院北京协和医院赵玉沛院士团队在《Clin Transl Med》发表的《Comparative spatial transcriptomics of pancreatic cancer with ductal and acinar origins in mouse models》研究,采用Sox9-CreER小鼠(转录因子 Sox9 是胰腺导管细胞的特异性标志物),开发了导管细胞起源PDAC---KrasLSL-G12D/+;Trp53FL/FL;Sox9-CreER(KPPS)小鼠模型。该模型可以模拟不同病理级别IPMN的发生,包括低级别(LG)、高级别(HG)和IPMN相关浸润性癌(IPMN-IC),表现出特征性的导管内肿瘤及腺管样胰腺癌的特征。
本研究通过基因编辑小鼠模型(KPPS小鼠、KPPC小鼠),结合致瘤特性、空间转录组学和多组学分析,揭示两种起源的PDAC在组织学、分子通路和免疫微环境上的差异,为胰腺癌更精准的研究,特别是针对IPMN与导管细胞起源的胰腺癌奠定了重要基础。此研究的KPPS小鼠的品系建立、扩繁和动物实验的服务由北京维通达提供。
部分实验设计与结果
(1)胰腺导管腺癌(PDAC)小鼠模型
a. 导管细胞起源PDAC:Sox9-CreER驱动的KPPS模型(基因型:KrasLSLG12D/+;Trp53fl/fl;Sox9-CreER),小鼠注射他莫昔芬(激活癌变开关),实验设计见图1A;
b. 腺泡细胞起源 PDAC:Pdx1-CreER驱动的KPPC模型(基因型:KrasLSL-G12D/+;Trp53fl/fl;Pdx1-CreER),小鼠注射他莫昔芬(激活癌变开关),实验设计见图1A。
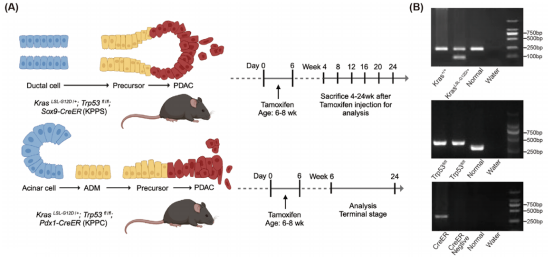
图1. 胰腺导管腺癌(PDAC)小鼠模型实验设计与基因型鉴定结果
(2)肿瘤病理学分析
研究者对KPPS和KPPC两种模型的胰腺进行H&E 染色,KPPS小鼠呈现不同级别IPMN的动态演进过程,包括低级别(LG)、高级别(HG)以及 IPMN 相关浸润癌(IPMN-IC),而KPPC表现出经典PDAC特征(图2 C-D)。
在他莫昔芬注射后12-24周,80%以上KPPS小鼠进展为浸润癌,呈现IPMN-IC与经典PDAC两种组织类型特征;KPPS小鼠的IPMN病变表现为非肠型IPMN亚型(包括胃型和胰胆管型)(图2 C-E)。
生存分析结果显示,KPPS小鼠的中位生存期为他莫昔芬处理后20周,显著长于KPPC小鼠的13周(图2 F)。
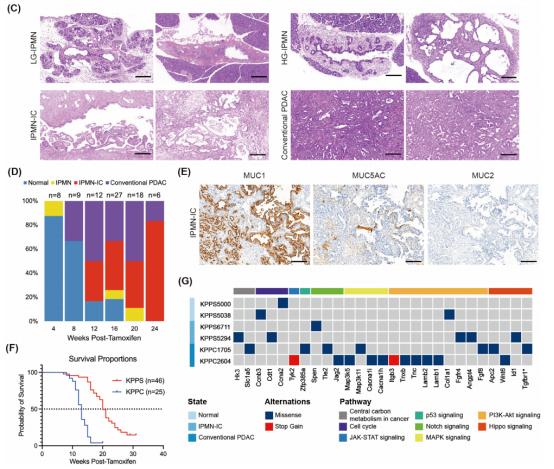
图2. 胰腺导管腺癌(PDAC)肿瘤特征对比
(3)空间转录学与免疫微环境分析
对肿瘤样本进行分析,对比肿瘤上皮和间质的基因表达差异。KPPS小鼠的上皮细胞高表达Tm4sf4和Cdh17,这两个基因或可作为识别导管细胞来源 PDAC的生物标志物(图3 D);而腺泡细胞特异性标志物(包括 Cel、Tff2等)在KPPC肿瘤中显著表达。值得注意的是, 模拟腺泡细胞起源的KPPC肿瘤周围的正常胰腺组织中角蛋白19(Krt19,导管细胞标志物)表达上调,这提示KPPC肿瘤邻近的正常胰腺组织可能在致病基因突变的作用下正在经历腺泡导管化生(ADM)过程(图 3D),而模拟导管细胞起源的KPPS肿瘤周围的正常胰腺组织没有观察到这一现象。
免疫谱分析显示,两种模型的肿瘤微环境均具有免疫抑制特征(图 3F、G)。与KPPC小鼠相比,KPPS小鼠的肿瘤微环境中树突状细胞(DCs)显著富集,尤其是静息态树突状细胞,同时浆细胞数量显著减少,提示两种不同类型的PDAC可能具有相近而又不完全相同的免疫微环境特征。
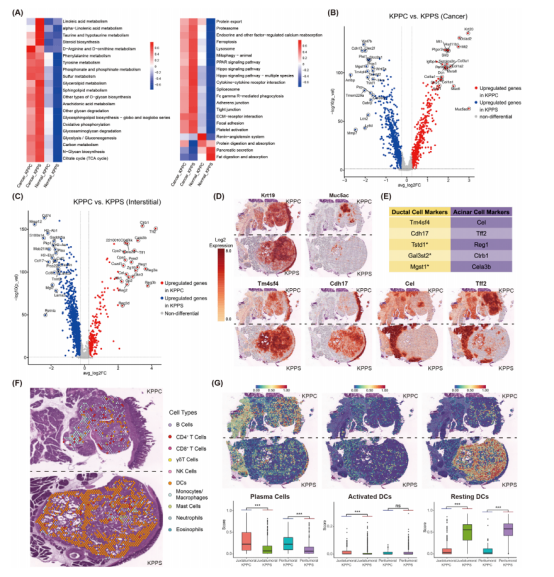
图3. 空间转录组学分析揭示了KPPS与KPPC模型中独特的肿瘤亚型及微环境特征
(4)临床相关性验证
为进一步评估研究的临床相关性,研究人员基于导管/腺泡标志物,将来自癌症基因组图谱(TCGA,全球知名癌症基因组数据库)的 178个人类PDAC数据集聚类分析。导管主导型人群与KPPS模型特征一致,高表达Tm4sf4和Cdh17,免疫微环境中 DCs 和抗原呈递通路富集,伴有MTOR、MYC、糖酵解及抗原呈递通路的上调;而腺泡主导型人群与KPPC模型特征一致,主要表现为KRAS、JAK-STAT与EMT通路的激活(见原文图3)。
总结
综上所述,KPPS模型可以成功模拟IPMN与导管来源PDAC的发生发展过程,其后期主要发展为IPMN相关浸润癌(IPMN-IC),并表现出胰胆管亚型的特征,具有重要临床模拟价值。KPPS模型中导管标志物(Tm4sf4、Cdh17)上调,而KPPC模型中腺泡标志物(Cel、Tff2 等)上调。这种与细胞起源相关的分子差异为 PDAC的分子亚型研究提供了新视角,有望为 PDAC的精准诊断、预后预测及治疗策略制定提供参考。
维通达提供胰腺癌相关模型和服务
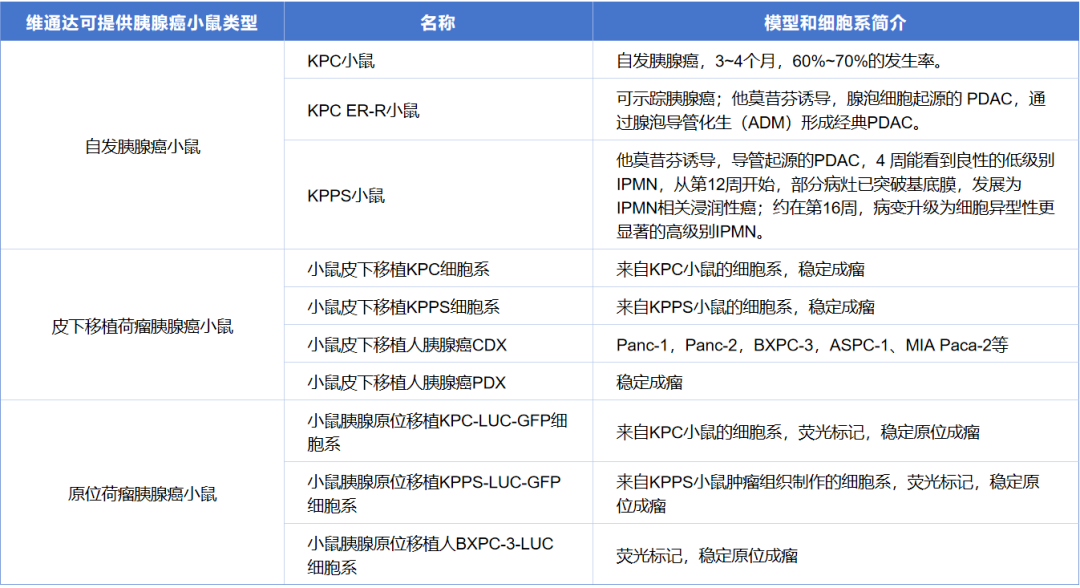
维通达可提供高度匹配临床病理特征的系列胰腺癌小鼠模型,全面覆盖不同发生类型、疾病阶段与组织起源,为胰腺癌机制研究与药物研发提供标准化临床前平台,助力靶向KRAS G12D的分子抑制剂、IPMN 癌前干预与化学预防药物、导管起源PDAC特异性靶向药、IPMN相关浸润癌的免疫治疗研发。维通达胰腺癌及药效服务包括:自发胰腺癌小鼠、诱导型胰腺癌小鼠(2月左右基本发生胰腺癌及其转移癌)、胰腺癌CDX模型建立和药效服务、胰腺癌PDX模型建立和药效服务等。